Noțiuni introductive
Datele de supravieţuire reprezintă timpul scurs de la începerea urmăririi unui subiect până la apariţia evenimentului, sau vârsta subiectului, la care se realizează evenimentul. (ex. timpul de la diagnosticarea cancerului ovarian până la deces, timpul de la aplicarea chimioterapiei în limfomul Hodgkin până la recădere)
Analiza datelor de supravieţuire este o colecţie de procedee statistice destinate prelucrării datelor de supravieţuire.
Datele de supravieţuire necesită o analiză statistică diferită de a datelor cantitative întrucât au nişte particularităţi. Astfel există informaţii incomplete (ex. subiecţi care la sfârşitul studiului nu realizează evenimentul predefinit (ex. vindecarea/decesul)). Informaţiile incomplete se numesc informaţii cenzurate. De asemenea distribuţia datelor de supravieţuire nu este una normală. Cenzurarea şi anormalitatea distribuţiei datelor de supravieţuire necesită metode statistice adecvate pentru analizarea lor corectă.
Datele de supravieţuire se descriu grafic prin curbe de supravieţuire. Metoda cea mai folosită de reprezentare este metoda Kaplan Meier. Curba de supravieţuire arată cum variază proporţia de pacienţi în viaţă (sau care nu au realizat evenimentul predefinit (deces/vindecare, ...)) în timp. Astfel se porneşte de la 100% supravieţuitori la începutul studiului, si acest număr scade pe măsură ce timpul trece.
Pentru a descrie supravieţuirea „medie” a subiecţilor dintr-un grup se utilizează mediana timpului de supravieţuire (întrucât datele nu sunt normal distribuite)
Pentru a evalua dacă există diferenţe între supravieţuirea unui grup şi a altui grup se utilizează testul log-rank (cel mai frecvent, în anumite situaţii se utilizează alte teste).
Pentru a prezice timpul de supravieţuire în funcţie de diferite caracteristici ale subiecţilor (ex. stadiul tumorii, tipul histologic, ...) se utilizează regresia Cox (cel mai frecvent, dar există şi alte metode). Tot regresia Cox se utilizează pentru a afla dacă o caracteristica a subiecţilor influenţează supravieţuirea, şi dacă da, cât de mult, şi în ce direcţie (o prelungeşte, sau o scurtează). Astfel, regresia Cox este utilă pentru evaluarea existenţei şi importanţei legăturii între un factor prognostic şi supravieţuire.
Pentru a evalua importanţa efectului unei caracteristici asupra supravieţuirii se utilizează rația hazardului (HR – hazard ratio). Rația hazardului se calculează pe baza hazardului.
Hazardul este riscul instantaneu al unui subiect de a realiza evenimentul prestabilit, dat fiind faptul că el a supravieţuit până în acel moment (ex. riscul instantaneu de a deceda, la un subiect cu melanom malign). Cu cât hazardul este mai mare, cu atât riscul de a deceda (sau realiza alt eveniment prestabilit) este mai mare (ex. o persoană care conduce maşina după ce a consumat alcool, are hazardul mai ridicat decât o persoană care conduce maşina dar nu a consumat alcool).
Rația hazardului unui grup de subiecţi faţă de un alt grup de subiecţi reprezintă raportul dintre hazardurile celor două grupuri de subiecţi (rația hazardului subiecţilor cu adenocarcinom pulmonar faţă de subiecţii cu cancer pulmonar epidermoid)
În această lucrare veţi exersa descrierea datelor de supravieţuire, veţi testa diferenţa între grupe diferite de subiecţi în ceea ce priveşte supravieţuirea, şi veţi evalua importanţa efectului unor caracteristici asupra timpului de supravieţuire.
Scenariul studiului-exemplu
Protocolul studiului
Pentru a răspunde la aceste întrebări, se vor citi diferite secţiuni (specificate pentru fiecare întrebare în parte) ale articolului cu titlul Effect of mitoxantrone on outcome of children with first relapse of acute lymphoblastic leukaemia (ALL R3): an open-label randomised trial, autori
Parker C, Waters R, Leighton C, et al. publicat în Lancet. 2010 Dec 11; 376(9757): 2009–2017. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3010035/
- Scop și obiective (Abstract & ultimul paragraf din Introduction)
Scop: Evaluarea efectului mitoxantronei comparativ cu idarubicina la copii cu leucemie acută limfoblastică a căror boală a recăzut sub regimurile de tratament actuale.
Obiectivele studiului:
- compararea supraviețuirii globale între mitoxantronă și idarubicina la copii cu leucemie acută limfoblastică a căror boală a recăzut sub regimurile de tratament actuale
- compararea supraviețuirii fără progresie între mitoxantronp și idarubicina la copii cu leucemie acută limfoblastică a căror boală a recăzut sub regimurile de tratament actuale
- Domeniul de cercetare: Evaluarea unei abordări terapeutice
- Tipul sudiului: (Methods)
- În funcţie de obiectivele studiului:
- Analitic (se fac teste, comparaţii, se caută legături, asocieri);
- În funcţie de rezultatele vizate / intervenția cercetătorului asupra subiecţilor şi evoluţiei bolii studiate):
- Experimental (cercetătorul intervine administrând preparate farmaceutice pentru a influența evoluția bolii);
- În funcţie de design:
- Cu grupuri paralele (fiecare subiect e alocat unui singur grup, pe toată durata studiului: mitoxantronă vs. idarubicină);
- În funcţie de obiectivul trialului:
- Trial de eficiență terapeutică / trial pragmatic (trial realizat în condiţii asemănătoare cu cele din viața curentă, incluzând eventualele probleme de complianță la tratament a pacienților);
- În funcţie de ipoteză clinică:
- Trial de superioritate (ipoteza trialului este că mitoxantrona e superioară față de idarubicină);
- În funcţie de faza de dezvoltare a medicamentului:
- Trial de Faza IV (Faza de farmacovigilenţa / postmarketing – după lansarea (aprobarea) pe piaţă a ambelor medicamente.).
În funcţie de metodele utilizate pentru asigurarea validității studiului prin evitarea erorilor sistematice (bias) și a factorilor de confuzie (confounders):
- Trial randomizat: subiecţilor le-au fost alocate la întâmplare (aleator/randomizat) cele două tratamente comparate. ” open-label randomized trial”
- Trial cu alocare mascată („allocation concealed” - cel care a introdus subiecţii în studiu nu a știut ce intervenţie va primi pacientul – Randomisation and masking - ”which enabled allocation concealment”);
- Trial în intenție de a trata: toţi pacienţii au fost analizaţi în grupurile în care au fost randomizaţi (analiza a fost de tipul “intenţie de a trata” („intention to treat analysis” – indiferent dacă au primit mitoxantronă sau idarubicină, chiar dacă nu au luat tot tratamentul, sau dacă l-au luat discontinuu, pacienții au fost analizaţi ca şi cum ar fi luat tratamentul în mod corect);
- Trial deschis (open label): nu a fost folosită metoda orb (blind/masking/mascare) – atât pacientul cât și investigatorul a știut ce primește ” open-label randomized trial”);
- Trialul a fost controlat (tratamentul evaluat a fost comparat cu idarubicină).
- Populaţia accesibila şi eşantionul de studiu (Methods)
Populaţia ţintă
- Caracteristici clinice (ex. boala, stadiul bolii, complicaţii, stare funcţională): Pacienți la prima recidivă a leucemiei acute limfoblastice care nu au primit transplant de măduvă, aflte în prima remisiune completă
- Caracteristici demografice (restricţii pe anumite vârste, sex, status socioeconomic, regiuni geografice): Copii (”Patients aged 1–18 years”)
Populaţia accesibilă
Pacienți din 22 de centre participante ale Grupului pentru copii și de leucemie (CCLG) din Regatul Unit și Irlanda. În noiembrie 2006, nouă centre din grupul de hematologie / oncologie din Australia și Noua Zeelandă (ANZCHOG) s-au alăturat studiului.
Eşantionul de studiu
Criterii de includere
Pacienți în vârstă de 1-18 ani, la prima recidivă a leucemiei acute limfoblastice care nu au primit transplant de măduvă, aflte în prima remisiune completă
Criterii de excludere
Cei cu leucemie limfatică limfoblastică acută B-matură
Talia (mărimea) eşantionului:
Cercetătorii au calculat o talie minim necesară pentru acest studiu, pe baza următoarelor considerente: putere de 80% pentru a detecta o creștere de 10% (90% față de 80%) în MRDlo la TP1 între brațele randomizate, utilizând un nivel de semnificație de 5%, pentru un test bilateral, cu un timp de angajare de 6-7 ani. Astfel ei au calculat că ar fi necesari 219 pacienți în fiecare braț al studiului.
- Modalitatea de culegere a datelor
- În funcţie de populaţia cuprinsă în studiu: Prin eşantionare (se studiază o parte din toată populaţia ţintă) ;
- În funcţie de durata culegerii datelor: Longitudinală, prospectivă (se culeg informaţii urmărind subiecţii în timp: la intrarea în studiu şi apoi după un interval de timp, pentru a înregistra evoluţia stării de pacienților);
- În funcţie de modul de alcătuire a grupului / grupelor de subiecţi luaţi în studiu: ~Eşantion reprezentativ – serie consecutive de pacienți (se studiază un eșantion de pacienți cu aceleași caracteristici / criterii de includere, care copiază fidel caracteristicile populaţiei din care a fost extras. Acest eșantion reprezentativ a fost apoi randomizat în mod mascat, dând naștere celor două grupuri comparate: grupul/lotul experimental).
- Definirea efectului studiat și a variabilelor asociate
Efectele studiate:
Principalele efecte studiate au inclus:
Supraviețuirea fără progresie a fost rezultatul principal. Supraviețuirea fără progresie a fost definită ca timpul scurs de la randomizare până la prima insuficiență de inducție (5% blaști sau mai mult în măduva osoasă la primul moment de evaluare, persistența blastilor CSF, non-regresia măririi testiculare), recădere, deces din orice cauză sau o a doua malignitate.
Supraviețuirea globală, a fost rezultat secundar. (definită ca timpul de la randomizare până la deces din orice cauză.)
Variabilele studiate (sunt menționate numai variabilele relevante scenariului de studiu propus spre rezolvare)
Variabile calitative (atribut): tipul tratamentului, statusul cenzurii.
Variabile de supraviețuire: timpul până la progresia bolii, timpul de supraviețuire.
- Planul de descriere şi analiză a datelor (sunt menționate numai metodele de descriere și analiză a efectelor și variabilelor urmărite și în scenariul de studiu propus spre rezolvare)
Planul de descriere a datelor
- Pentru variabile calitative: tabele de frecvență;
Planul de analiză a datelor
Analiza prin tabele sau figuri a relaţiei dintre variabile:
- Autorii studiului au utilizat grafice de tip Kaplan-Meier pentru a prezenta evoluția probabilității de supraviețuire în timp, în funcție de tratament
Analiza statistică în funcție de obiectivele acesteia:
- Evaluarea existenţei efectului terapeutic
- Testul log-rank - pentru compararea supraviețuirii dintre cele două loturi studiate;
- Cuantificarea eficienței terapeutice (numai dacă la obiectivul anterior se poate dovedi existența unui efect terapeutic semnificativ statistic)
- Estimatorii punctuali şi intervalele de încredere (95% CI) ale unor indicatori medicali de cuantificare a eficienței terapeutice:
- Rația hazardului (hazard ratio): HR, obținută prin regresia Cox.
- Probabilitatea de supraviețuire la 3 ani în ce privește supraviețuirea fără progresie, respective supraviețuirea globală
- Timpul median de supraviețuire
Instrumente de analiză utilizate: STATA software release 7 (StataCorp, College Station, Texas, USA)
Rezultate obținute în studiu. Analiza datelor și prezentarea lor
În urma aplicării criteriilor de includere și excludere impuse în planul de studiu, din 239 potențiali participanți evaluate introduși consecutive în studiu, doar 216 au putut fi incluși în studiu și randomizați în cele două loturi studiate (vezi figura 2 din articol).
Grupurile randomizate s-au dovedit a avea caracteristici comparabile (vezi tabelul 2 din articol – procente - similare, valorile medianelor - similare).
Mediana timpului de urmărire (median follow-up) a fost de 41 de luni în cele două grupuri (95% CI 34-48).
La trei ani, proporția supraviețuirii globale a fost de 57,1% (95% CI 49,5-63,9), respectiv proporția supraviețuirii fără progresie a fost de 50,3% (95% CI 42,9-57,3). Grupul care a primit mitoxantronă a avut proporția supraviețuirii globale de 69,0% (95% CI 58,5-77,3) (vezi fig. 1), respectiv proporția supraviețuirii fără progresie de 64,6% (95% CI 54,2-73,2), iar grupul care a primit idarubicină: 45,2% (95% CI 34,5-55,3), respectiv 35,9% (95% CI 25,9-45,9).
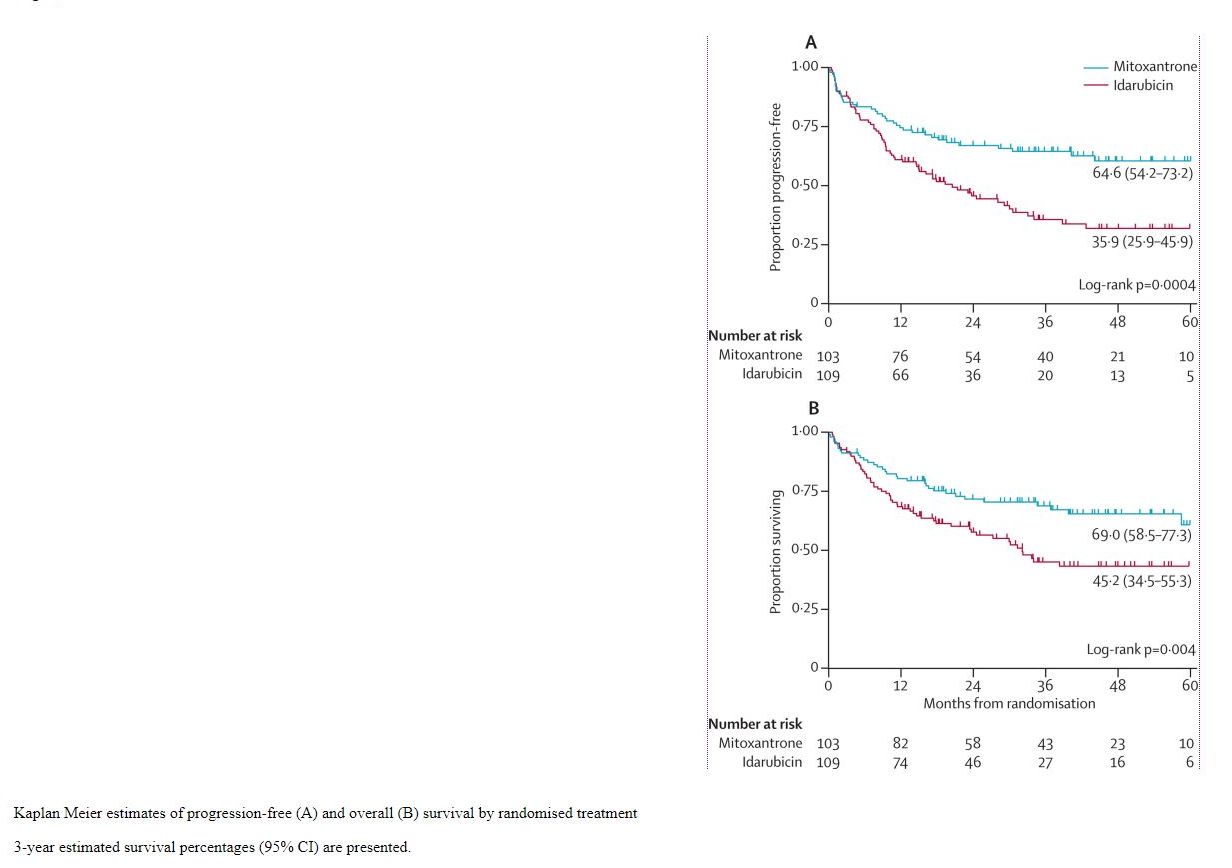
Fig. 1 Evoluția supraviețuirii globale comparativ între copii cu leucemie acută limfoblastică ce au primit mitoxantronă (albastru), respectiv idarubicină (roșu)
Testul log-rank pentru a compara supraviețuirea globală a oferit un p=0,0004, respectiv pentru a compara supraviețuirea fără progresie a oferit un p=0,004.
În urma analizei Cox multivariate (ajustând pentru efectul altor variabile de confundare) s-a obținut rația hazardului (mitoxantronă vs. idarubicin) pentru supraviețuirea globală de 0,56 (95% CI 0,36-0,87), p=0,01, respectiv 0,54 (95% CI 0,36-0,82), p=0,003.
Interpretarea rezultatelor. Discuții
Interpretarea statistică
Mediana timpului de urmărire – 50% din subiecți au fost urmăriți cel puțin 41 de luni, sau 50% din subiecți au fost urmăriți mai puțin de 41 de luni.
Proporția supraviețuirii globale la 3 ani pentru grupul tratat cu mitoxantronă – 69% dintre subiecții care care au primit mitoxantronă la 3 ani erau încă în viață
Diferența de proporție a supraviețuirii globale la 3 ani dintre grupul tratat cu mitoxantronă și cel tratat cu idarubicină – 69%-45,2%=23,8% - dintre subiecții care care au primit mitoxantronă la 3 ani erau încă în viață cu 23,8% mai mulți subiecți decât cei care au primit idarubicină
Proporția supraviețuirii fără progresie la 3 ani pentru grupul tratat cu mitoxantronă – la 64,6% dintre subiecții care care au primit mitoxantronă la 3 ani boala nu a progresat
Testul log-rank pentru a compara supraviețuirea globală – există o diferență statistic semnificativă între supraviețuirea globală între cei care au primit mitoxantronă și cei care au primit idarubicină (pentru că p=0.004 0.05, respingem ipoteza nulă și acceptăm ipoteza alternativă. Ipoteza nulă: nu există o diferență statistic semnificativă între supraviețuirea globală între cei care au primit mitoxantronă și cei care au primit idarubicină. Ipoteza alternativă: există o diferență statistic semnificativă între supraviețuirea globală între cei care au primit mitoxantronă și cei care au primit idarubicină).
Rația hazardului în ce privește supraviețuirea globală, estimatorul punctual – hazardul grupului care a primit mitoxantronă de a realiza evenimentul prestabilit (decesul) este de 0,56 ori mai mare față de grupul care a primit idarubicină, după ajustarea pentru efectul celorlalte variabile. Întrucât 0,56 este mai mic decât 1 și pentru că evenimentul prestabilit este unul negativ (decesul) înseamnă că grupul care a primit mitoxantronă are hazard mai mic și astfel supraviețuirea mai bună decât grupul care a primit idarubicină. Acest rezultat este un estimator punctual, adică reprezintă pe de o parte valoarea rației hazardului în studiu (pe datele culese), dar pe de altă parte este și cea mai bună estimare pe care o avem legat de ce se petrece în populația țintă, în realitate (dacă eșantionul este reprezentativ).
Rația hazardului în ce privește supraviețuirea globală, intervalul de încredere – adevărata valoare a rației hazardului în populația țintă se află între 0,36 și 0,87 cu o probabilitate de 95%.
Aprecierea preciziei rației hazardului în ce privește supraviețuirea globală – pentru evaluarea preciziei ne uităm la lărgimea intervalului de încredere – între 0,36 și 0,87. Putem considera intervalul între 0 și 1 ca un interval între 0% și 100%. Valoarea 1 înseamnă că nu există diferențe în ce privește hazardul celor 2 grupuri. Astfel valorile apropiate de 1 indică diferențe mici de hazard între grupuri, respectiv valorile îndepărtate de 1 indică diferențe mari. Astfel 0,87este situat la 13% față de 1 (100-0,87=13), respective 0,36 este situat la 64% față de 1. Putem considera intervalul între 13% și 64% relative larg, astfel, rezultatul este relativ imprecis.
Interpretarea clinică
Diferența de proporție a supraviețuirii globale la 3 ani dintre grupul tratat cu mitoxantronă și cel tratat cu idarubicină – 69%-45,2%=23,8% – 23,8% mai mulți subiecți în viață este un rezultat clinic important – fiind vorba de decese prevenite.
Rația hazardului în ce privește supraviețuirea globală, estimatorul punctual - 0,56 sugerează o înjumătățire aproape a hazardului a grupului care primește mitoxantronă față de grupul care primește idarubicină. Mai putem privi rezultatul și sub forma unei diferențe de 44% față de valoarea 1. Putem astfel considera că rezultatul este clinic relativ important
Rația hazardului în ce privește supraviețuirea globală, intervalul de încredere – un capăt al intervalului de încredere este situat la 13% față de 1, iar celălalt la 64% față de 1. 64% este relativ important. Pentru 13%, inițial putem să ne gândim că nu este clinic important, însă dacă ținem cont că este vorba de riscul de deces, atunci putem considera că 13% este relativ important clinic. Astfel ambele capete ale intervalului de încredere sunt clinic importante, putem considera că întreg intervalul de încredere este clinic important.
Concluzia studiului
Mitoxantronei comparativ cu idarubicina la copii cu leucemie acută limfoblastică a căror boală a recăzut sub regimurile de tratament actuale oferă un avantad în ce privește supraviețuirea globală și o supraviețuirea fără progresie, statistic semnificativă și clinc importantă.
De reținut
Datele de supravieţuire reprezintă timpul scurs de la începerea urmăririi unui subiect până la apariţia evenimentului.
Întrucât datele de supraviețuire nu sunt normal distribuite și există fenomenul cenzurării, pentru descriere se folosește mediana timpului de supraviețuire, grafice de tip Kaplan-Meier, pentru comparație testul log-rank și pentru predicție – regresia Cox cu rația hazardului.
Hazardul este riscul instantaneu al unui subiect de a realiza evenimentul prestabilit, dat fiind faptul că el a supravieţuit până în acel moment, fiind invers proporțional cu supraviețuirea.


